Feuer und Flamme
Vorbemerkung:
1. Entzünden von heißem Wachs mit kaltem Wasser
2a. Unter welchen Bedingungen brennt Wachs?
2b. Erhitzen von Wachs im Reagenzglas
2c. Erhitzen von unverbranntem Wachsdampf (Tochterflamme)
2d. Entflammen von unverbranntem Wachsdampf
2e. Brennen auch
bei Holz, Papier etc. nur die entweichenden Gase?
2f. Entflammen von Leichtbenzin, Alkohol und Petroleum
2g. Warum ist die Farbe der Flamme fast immer gelb?
3a. Bei welcher Temperatur entzündet sich ein Streichholz?
3b. Wann entflammt Erdgas bzw. Feuerzeuggas?
3c. Der Papiertrichter über der Kerzenflamme
4a. Ist die Menge des brandfördernden Stoffes wichtig?
4b. Die Wirkung der Oberfläche für den brandfördernden Stoff
4c. Brennender und brandfördernder Stoff als Gasgemisch
4d. Ist die Art des brandfördernden Stoffes wichtig? Experimente mit Sauerstoff
4e. Wird Eisen beim Verbrennen schwerer?
4f. Wie viel Sauerstoff ist in der Luft?
4g. Spezialfall: Wasserstoff und Sauerstoff
4h. Chemisch gebundener Sauerstoff: Gummibärcheninferno
5a. Die Rolle des Dochtes
5b.Temperaturverteilung
5c. Was geschieht chemisch (Nachweis von C als CO2 und von H als H2O)
5d. Wird die Kerze (incl. Produkte) beim Verbrennen leichter?
6a. Das Branddreieck
6b. Beispiele für Feuer löschen
6c. Löschen mit Kohlenstoffdioxid
6d. Löschen von Benzinbränden
6e. Experimente mit der Kupferspirale
6f. Wer baut den besten Feuerlöscher
7. Vermischtes oder Gelerntes
7a. Erlischt die untere oder die obere Kerze zuerst?
7b. Feuerspucken
7c. Feuertornado
7d. Feuerspirale
7e. Benzinexplosion im Filmdöschen
7f. Feuerzeuggas-Rakete
Vorbemerkungen
Zu diesem hier behandelten Thema gibt es eine Fülle von Versuchen, die man als Demonstrations-, Schülerdemonstrations- oder reine Schülerexperimente durchführen kann. Früher konnte man in den Lehrbüchern immer nur einzelne Passagen hierzu finden. Es wurde deshalb ein eigener Unterrichtsgang konzipiert, der an der eigenen Schule mehrfach erprobt wurde und hier vorgestellt werden soll.
"Aufgepeppt" wurde die Reihe nachträglich noch mit Experimenten aus folgenden Artikeln:
1. "Die Kerze", W. Helmert und Dr. A. Salinger,
Berlin 1999 (http://home.snafu.de/helmert
/Kerze/index.htm)
2. "Chemie fürs Leben", Marco Rossow, Prof Dr. Alfred Flint Stand Nov.
2005 Universität Rostock,
Institut für Chemie
Die Unterrichtsreihe immer wieder modifiziert und in NRW mit Erfolg beschritten. Platziert war sie in der Mitte der Klasse 7 nach der Reihe über den Kalkkreislauf.
Da an nicht allen Schulen in den verschiedenen Bundesländern die gleichen Voraussetzungen bzw. Hauscurricula vorhanden sind, um genau den gleichen Weg zu gehen, muss eventuell die eine oder andere Passage (s.u.) abgeändert werden.
Als zusätzliche Hilfe zu dem didaktischen Vorschlag finden sich auf der rechten Seite der Darstellung Links zu Hilfen wie Filmen oder Arbeitsblättern.
Aus einem Schülerheft (etwas überarbeitet)
Nachdem wir genügend gedrängelt hatten, hat der Lehrer zugesagt, dass wir etwas mit Feuer als nächstes machen dürfen.
Was ich unter Feuer verstehe
-Wenn ich an Feuer denke, dann denke ich
Explosionen, Hitze, große Temperaturen, abfackelnde
Häuser und Waldbrände.
- Ich denke auch an Bunsenbrenner.
- Aber ich denke auch an Kerzen und wenn ich an Kerzen denke, denke ich auch an Licht."
|
Welche Bedingungen müssen erfüllt sein, damit es brennt? 1. Brennbares Material Benzin, Holz, Erdgas, Deospray, Papier Heu, Kohle, Wachs, Schwarzpulver Nicht brennbare Stoffe sind dagegen: Kohlenstoffdioxid, Wasser, Glas Löschdecke, Sand
2. Brandfördernde Stoffe Luft oder besser: Sauerstoff manche Chemikalien und Schwarzpulver ( ist auch bei Nr. 1 aufgeführt!)
3. Feueranzünder |
Der Lehrer sagt: "Ihr habt eigentlich alles so toll zusammengetragen, dass wir die Unterrichtsreihe gar nicht mehr durchzunehmen brauchen; aber ich möchte mit Euch noch ein paar Feinheiten genauer herausarbeiten. Ich sehe schon am Leuchten in euren Augen dass es viel Spaß machen wird."
Versuch: (wird vom Lehrer durchgeführt)
1. Entzünden von heißem Wachs mit kaltem Wasser
|
Prinzip: |
Es wird ein Reagenzglas mit erhitztem Wachs in kaltes Wasser gehalten. |
||
|
Skizze: |
entfällt |
 Film:
A14A Film:
A14A |
|
|
Material: |
Schutzbrille, Bunsenbrenner, Gasanzünder, Reagenzglas, Reagenzglashalter Spatel, Becherglas, 600 mL |
||
|
Chemikalien: |
Kerze(nwachs), Leitungswasser |
||
|
Durchführung Beobachtung: |
Wir befüllen das Becherglas etwa zu
dreiviertel mit kaltem Leitungswasser. Dann knicken wir eine
Weihnachtskerze so etwa bei 1-2 cm ab, ziehen das Wachs vom
Docht und geben es in das Reagenzglas. Der Lehrer zieht die
Schutzscheibe hoch und erhitzt das Reagenzglas in der
Brennerflamme, bis es eigenartig zischt. Dann stellt er den
Brenner ab und hält das Reagenzglas in das kalte Wasser. |
||
|
Ergebnis: |
Heißes Wachs brennt auch ohne Feueranzünder. |
||
Der Lehrer sagt: Dieses Experiment enthält einen
Trick, den er später erklären wird.
Wir sollen auf keinen Fall diesen Versuch irgendwie zu Hause
nachmachen!
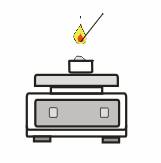
2a. Unter welchen Bedingungen brennt Wachs?
|
Prinzip: |
Wachs wird auf dem Magnetrührer erhitzt und versucht anzuzünden. |
||
|
Skizze: |
|
 Film: A14B |
|
|
Material: |
Magnetrührer, Schutzbrille, Spatel |
||
|
Chemikalien: |
Kerze(nwachs) im Teelichtbecher, Streichhölzer |
||
|
Durchführung Beobachtung: |
Wir entleeren ein Teelicht und stampfen
oder drücken den Boden glatt. Dann geben wir nur ein größeres Stück
Wachs zurück in den Teelichtbecher. Diesen stellen wir dann auf
den Magnetrührer und schalten ihn an. |
||
|
Ergebnis: |
Eigentlich brennt Wachs nur wenn es verdampft |
||
Den Versuch fanden wir nicht so eindeutig. Wir haben daraufhin diskutiert, wie man ihn verbessern könnte und kamen auf eine tolle Idee: Wir machen Wachs im Reagenzglas heiß und zünden dann den Dampf an.
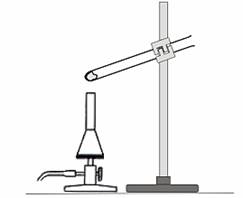
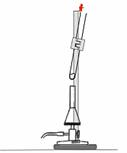
2b. Erhitzen von Wachs im Reagenzglas
|
Prinzip: |
Wachs wird im Reagenzglas erhitzt und versucht dieses anzuzünden. |
|
|
Skizze: |
|
 Film: A14D |
|
Material: |
Schutzbrille, Bunsenbrenner, Gasanzünder, Reagenzglas, Stativ, Muffe, Greifklemme |
|
|
Chemikalien: |
Kerze(nwachs) |
|
|
Durchführung Beobachtung: |
Wir knicken eine Weihnachtskerze etwa
bei 1 cm ab, ziehen das Wachs vom Docht und geben das Stück in
ein Reagenzglas. Dieses erhitzen wir in der rauschenden Flamme,
bis es flüssig wird und schließlich Wachsdampf entweicht. |
|
|
Ergebnis: |
Es brennt nur gasförmiges Wachs. |
|
2c. Entflammen von unverbrannten Wachsgas
| Skizze: |
 Film: A14C |
|
Durchführung Beobachtung: |
Eine Kerzenflamme, die stabil ist (d.h. schon einige Minuten gebrannt hat), wird ausgepustet. Man nähert sich dem aufsteigenden Rauch mit einem brennenden Streichholz. Die Flamme entzündet den Qualm und springt von da aus auf den Docht über! Der Versuch ist fast beliebig oft wiederholbar. |
2d. Erhitzen von unverbranntem Wachsgas (Tochterflamme)
 |
|
|
Durchführung Beobachtung: |
Mittels kurzer Glasröhrchen werden noch nicht
verbrannte Gase aus einer Flamme abgeleitet und am Ende des Glasrohres
entzündet. Es bilden sich Flammen aus, die in der Struktur (innerer
Kegel etc.) der Ausgangsflamme entsprechen. |
Was mit dem Wachs passiert, könnte natürlich erst recht mit Alkohol oder Benzin geschehen; vielleicht sogar mit Holz.
2e. Brennen auch
bei Holz, Papier etc. nur die entweichenden Gase/Dämpfe?
|
Prinzip: |
Brennbare Stoffe werden im Reagenzglas erhitzt und versucht anzuzünden. |
|
Skizze: |
wie bei Versuch 2a |
|
Material: |
wie bei Versuch 2a |
|
Chemikalien: |
Holz (Schaschlik-Spieße), Papier, Alkohol usw. |
|
Hinweis: |
VORSICHT: Bei der eintretenden
Verkohlung können giftige und kanzerogene Stoffe entstehen!
ABZUG! |
|
Durchführung Beobachtung: |
Wir geben gruppenweise den brennbaren Stoff in das Reagenzglas. Dieses erhitzen wir in der rauschenden Flamme und halten den Reagenzglasrand kurz in die Brennerflamme. In allen Fällen können wir das entweichende Gas anzünden. Manchmal stinkt es dabei und die Stoffe werden schwarz und teerig. |
|
Ergebnis: |
Bei brennbaren Stoffen brennt nur das entweichende Gas. |
Fazit: Flammen sind brennende Gase!
Unser Lehrer ist zwar stolz auf uns, aber immer
noch nicht zufrieden: Er dreht den Gashahn am Brenner auf und sagt:
"Hier haben wir doch Gas. Warum brennt es nicht?"
|
Durchführung Beobachtung: |
Der Lehrer fuchtelt mit dem Gasanzünder weit über der Brenneröffnung und daneben herum. Die Funken aus dem Gasanzünder sprühen, aber das Gas entzündet sich an keiner der genannten Stellen. Auch auf dem Tisch unter halb des Brenners kann er das Gas nicht entzünden. Erst wenn die Funken in die Nähe der Brenneröffnung kommen entzündet sich das Gas. |
|
Ergebnis: |
Auch Erdgas lässt sich nur entzünden, wenn dessen Menge (besser: Konzentration) genügend groß ist. |
Nun ist uns klar, dass Gas vorhanden sein muss. Aber wie entsteht das Gas, wenn der Stoff noch nicht brennt
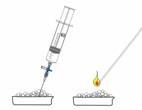
2f. Entflammen von Leichtbenzin, Alkohol und
Petroleum
|
Prinzip: |
Kleine Portionen der Stoffe werden auf den Experimentiertisch gegossen und versucht anzuzünden. |
|
|
Skizze: |
entfällt |
 Film: A14G |
|
Material: |
Schutzbrille, Bunsenbrenner, Gasanzünder, Streichhölzer |
|
|
Chemikalien: |
Leichtbenzin (Siedebereich 40-60°C), Alkohol (Ethanol) und Petroleum |
|
|
Durchführung Beobachtung: |
1. Ein Mitschüler verteilt auf unserem Kacheltisch mit der Spritze 0,5 mL Leichtbenzin. Wir sehen schon, wie sich die Lache verkleinert weil das Benzin verdunstet. Wir entzünden es schnell mit einem Streichholz vom Rand her. Es entzündet sich bereits, wenn das brennende Streichholz ca. 20 cm entfernt ist. Es bildet sich eine eindrucksvolle Stichflamme, die weit über die Größe der Lache hinausgeht. Das Benzin brennt schnell ab. 2. Genauso geben wir mit der Spritze 0,5 mL Alkohol
auf die Kacheln und
zünden ihn an. Er entzündet sich erst, wenn das brennende
Streichholz die Lache berührt. |
|
|
Ergebnis: |
Die Stoffe lassen sich verschieden leicht entzünden, weil sich bei Zimmertemperatur unterschiedlich viel Dampf über der Flüssigkeit bildet. Wenn der Dampf brennt, verdampft die Hitze wieder Flüssigkeit usw. |
|
2g. Warum ist die Farbe
einer Flamme fast immer gelb
|
Prinzip: |
a) Es wird ein Magnesiastäbchen oder ein kaltes Reagenzglas über eine Kerzenflamme gehalten b) Es wird Ruß (Kohlestaub) in eine nichtleuchtende Flamme gestreut |
|
|
Skizze: |
entfällt |
|
|
Material: |
Schutzbrille, Bunsenbrenner, Gasanzünder, Reagenzglas, Spatel |
|
|
Chemikalien: |
Kerze, Bernnergas |
|
|
Durchführung Beobachtung: |
a) eine Kerze wird angezündet. Dann hält man quer ein Reagenzglas
darüber, dass sie stark rußt und hält darüber einen
Bunsenbrenner mit rauschender Flamme. Kommt der Ruß in die
Flamme färbt sie sich sofort gelb. Hält man das angeschwärzte Magnesiastäbchen in die rauschende Flamme wird es wieder weiß. b) mit einem Spatel werden feine Kohlestaubteilchen in die rauschende (entleuchtete) Flamme eines schräg gestellten Brenners gestreut: Sie beginnt augenblicklich an den Stellen, wo Kohleteilchen hingelangen, zu leuchten. |
|
|
Ergebnis: |
Die Flamme färbt sich gelb, weil fast alle Brennstoffe Kohlenstoff enthalten: Wenn diese unvollständig (mit ungenügend Sauerstoff)verbrennen, dann glüht der entstehende Kohlenstoff in der Flamme auf. Auf dem Glühen beruht die gelbe Falmmenfarbe. |
|
Unser Lehrer ist immer noch nicht zufrieden: "Am Brennerkopf haben wir doch genügend Gas. Warum brennt es nicht von alleine?" Judith erinnerte ihn, dass wir schon in der Stunde davor festgestellt hatten, dass man einen Gasanzünder benötigt. Aber warum brannte das Wachs im Versuch 1, ohne das es angezündet wurde? Das muss irgendwas mit der Höhe der Temperatur zu tun haben. Wir wollen dies untersuchen an einem Stoff, der sich schon nur durch Reibung entzündet: an Streichhölzern
|
3a Bei welcher Temperatur entzündet sich ein Streichholz? Der Versuch gelingt so nicht mit Holz oder Papier im Reagenzglas !! |
3b. Wann entflammt Erdgas bzw. Feuerzeuggas?
3c. Kann man Papier mit einer Kerze entflammen?
 Film: A14K |
|
|
Durchführung / Beobachtung: |
Ein Teelicht wird unter einen
Papiertrichter gestellt: Er geht in Flammen auf. |
|
Ergebnis: |
Mit Wasser kann man Papier unter seinem Flammpunkt gekühlt halten. |
Tabelle einiger Substanzen
| Substanz | Siedepunkt | Flammpunkt | (Selbstent-)Zündtemperatur |
| [°C] | [°C] | [°C] | |
| Wasserstoff | -253 | 465 | |
| Methan (Erdgas) | -162 | 595 | |
| Acetylen (Schweißgas) | -84 | 305 | |
| Propan (Feuerzeug) | -42 | 470 | |
| Butan (Feuerzeug) | 0 | 365 | |
| Aceton | 56 | -18 | 540 |
| Methanol | 65 | 11 | 455 |
| Ethanol (Brennspiritus) | 78 | 13 | 425 |
| n-Heptan (ROZ=0) | 98 | -4 | 215 |
| Isooctan, 2,2,4-Trimethylpentan (ROZ=100) | 99 | -12 | 410 |
| Streichholzkopf | 80-160 | ||
| Zeitungspapier | 175 | ||
| Stroh | 250-300 | ||
| Holz | 270-340 | ||
| Wachs | 400 |
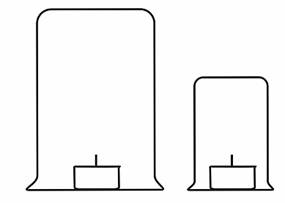
4a.
Ist die Menge des brandfördernden Stoffes
wichtig?
|
Prinzip: |
Zwei Teelichte werden unter unterschiedlich großen Bechergläsern gleichzeitig entzündet, um die Rolle der Umgebungsluft zu studieren |
|
Skizze: |
|
|
Material: |
Schutzbrille, Becherglas 600 mL, Becherglas 250mL, Streichhölzer |
|
Chemikalien: |
2 Teelichte |
|
Durchführung Beobachtung: |
Die Teelichte werden angezündet und die Bechergläser darüber gestülpt. Man kann beobachten, dass die Kerze unter dem kleinen Becherglas zuerst verlischt. Offensichtlich ist bei sonst gleichen Bedingungen im großen Becherglas mehr Luft vorhanden |
|
Ergebnis: |
Feuer ist nicht nur von der Masse des Brennstoffes, sondern auch von der Menge des brandfördernden Stoffes abhängig. |
4b. Die Wirkung der Oberfläche für den brandfördernden Stoff
 Film: A14M |
|
|
Durchführung Beobachtung: |
In Versuch 2f brannte Petroleum eigentlich nur, wenn das Streichholz in der Nähe war. Nun sprühen wir das Petroleum mit einem Zerstäuber in die Brennerflamme: Es entsteht eine Stichflamme, |
| Ergebnis: | Die Oberfläche wird durch das Zerstäuben so groß, dass sich genug Gas bildet ist und genügend Luftsauerstoff herankommt. |
4c. Brennender und brandfördernder Stoff als Gasgemisch
 Film: A14N |
|
|
Durchführung Beobachtung: |
In einem Automotor wird der brennbare Stoff gasförmig gemacht und mit Luft vermischt. Dies geschieht im Vergaser. Die Zündung erfolgt im Modellmotor |
| Ergebnis: | Benzin-Luft-Gasgemische reagieren bei Zündung explosionsartig und können einen Kolben treiben. |
4d Ist die Art des brandfördernden Stoffes wichtig? Experimente mit Sauerstoff
Exkurs:
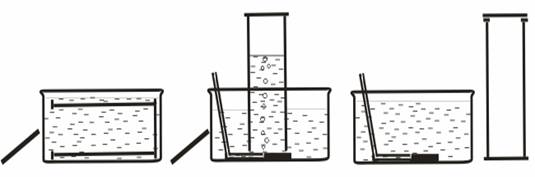
pneumatisches Auffangen von Gasen
|
Prinzip: |
In einen mit Wasser gefüllten Standzylinder wird ein Gas eingeleitet. |
|
Skizze: |
|
|
Material: |
Pneumatische Wanne, Standzylinder, Gaseinleitungshilfe, Deckglas |
|
Chemikalien: |
Gas (z.B. Sauerstoff) |
|
Durchführung Beobachtung: |
Die pneumatische Wanne wird mit Wasser gefüllt und die Einleitungshilfe hinein gestellt. Dann wird der Standzylinder vollständig mit Wasser gefüllt und umgekehrt auf die Einleitungshilfe gestellt. Schließlich wird Gas eingeleitet. Es steigt im Messzylinder hoch, bis dieser vollständig gefüllt ist. Zum Abschluss wird der Zylinder unter Wasser mit dem Deckglas verschlossen und aufrecht hingestellt. |
|
Ergebnis: |
Jedes wasserunlösliche Gas verdrängt auf Grund seiner viel kleineren Dichte das Wasser aus dem Standzylinder. Dieser kann so vollständig gefüllt werden. (Gasometer) |
Experimente mit reinem Sauerstoff
 Film: A14H |
|
|
Durchführung / Beobachtung: |
Eine Kerze, .Eisenwolle und Holzwolle werden entzündet und in einen mit Sauerstoff gefüllten Standzylinder gehalten. |
|
Ergebnis: |
A Kerze in Luft brennt normal ---- in reinem Sauerstoff viel heller
B Eisenwolle in Luft glüht normal ---- in reinem Sauerstoff heller
C Holzwolle in Luft brennt normal ---- in reinem Sauerstoff viel heftiger Glühende Holzwolle entzündet sich in reinem Sauerstoff |
Mit der entflammenden Holzwolle haben wir einen
schönen Test auf Sauerstoff gefunden. Wir füllen das zu testende Gas in
ein Reagenzglas (Öffnung nach oben) und halten einen glimmenden
Span hinein.
|
Glimmspanprobe |
Hält man einen glimmenden Span in ein mit Gas gefülltes Reagenzglas und entflammt dieser, so ist Sauerstoff vorhanden. |
Der Lehrer sagt: "Kerzenbrand kennt Ihr, auch das Holzwolle brennt aber- das Eisen brennt ist für die meisten von Euch neu. Wird nun das Eisen schwerer beim Erhitzen oder leichter?"
Wir stimmen ab. Alle sind dafür, dass es leichter wird.
De Lehrer: "Ist keiner von euch mutig?"
Wir: "Wieso, wir haben Ahnung!"
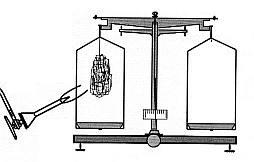
4e Wird Eisen beim Verbrennen schwerer?
|
Prinzip: |
Eisenwolle wird an einer Balkenwaage verbrannt und dabei gewogen. |
|
Skizze: |
|
|
Material: |
Balkenwaage, Gasbrenner, Anzünder |
|
Chemikalien: |
Eisenwolle |
|
Durchführung Beobachtung: |
Die Eisenwolle wird an der Waage befestigt. Dann wird die Waage austariert. Erhitzt man die Eisenwolle mit dem Gasbrenner, so scheint die Waage auf der Eisenseite zunächst hochzugehen. Das Eisen glüht auf und die Farbe ändert sich von metallisch glänzend in schwarz. Die Schale senkt sich immer mehr nach unten. |
|
Ergebnis: |
Eisen wird beim Verbrennen schwerer |
Schade, wir haben alle verloren.
Der Lehrer teilt uns mit, dass
diese Reaktion ausgenutzt werden kann, um den Sauerstoffgehalt der Luft
zu bestimmen. Dazu brauchen wir eine abgeschlossene Apparatur
veränderlichen Volumens.
|
4f Wie viel Sauerstoff ist in der Luft? AB A04
|
|
Ergebnis: |
In der Luft befinden sich etwa 20% Sauerstoff |
4g Spezialfall: Verbrennen von Wasserstoff mit Sauerstoff
|
Skizze: |
|
|
Ergebnis: |
A Wasserstoff in Seifenblasen brennt ruhig ab B Wasserstoff mit Luft gemischt in Seifenblasen knallt beim Anzünden C Wasserstoff mit Sauerstoff gemischt in Seifenblasen: Ein Riesenknall |
Lehrer:"Das ist die Vorstufe zum Wasserstofftest: Die Knallgasprobe" (Reagenzglas Öffnung nach unten)
|
Knallgasprobe |
Wenn man ein gasgefülltes Reagenzglas einer Flamme nähert und es eine kleine
Explosion (
"Plop" bzw. "Puii")
gibt, so handelt es sich bei dem Gas um Wasserstoff
|
Der brandfördernde Stoff kann nicht nur aus der Luft (oder aus der Gasflasche wie beim Schweißen) kommen sondern kann auch aus Stoffen freigesetzt werden.
4h Chemische Stoffe können Sauerstoff
freisetzen: Gummibärcheninferno
|
Prinzip: |
Gummibärchen sollen mit Sauerstoff auf Kaliumchlorat reagieren. |
|
|
Skizze: |
|
 Film A14L |
|
Material: |
Schutzbrille, Bunsenbrenner, Gasanzünder, großes Reagenzglas, Stativ, Muffe, Greifklemme |
|
|
Chemikalien: |
Gummibärchen, Kaliumchlorat |
|
|
Durchführung Beobachtung: |
Raum abdunkeln! In einem ganz leicht schräg eingespannten Reagenzglas erhitzt man rund 10 g Kaliumchlorat bis zum Schmelzen. Unmittelbar danach gibt man das Gummibärchen hinzu, welches sofort unter heftigem Tanzen mit einer bläulichen Farbe verbrennt. Begleitet wird der Vorgang von einem kräftigen Brummen und Zischen. |
|
|
Ergebnis: |
Der aus dem Kaliumchlorat freigesetzte Sauerstoff reagiert mit der Gelatine des Gummibärchens unter Feuererscheinung. Die bei der Verbrennung entstehenden Gase reißen das Gummibärchen periodisch mit sich und verursachen so den Tanzeffekt |
|
5a. Die Rolle des Dochtes
Wie funktioniert eine Kerze bzw. Petroleumlampe
Das ist doch klar: "Es liegt nur am Docht!!" ........aber...........
|
Skizze: |
|
|
Durchführung Beobachtung: |
Brennprobe: Der Docht brennt gar nicht richtig er glimmt nur. Chromatographietest: Hält man den Docht z.B. in
eine Kristallviolettlösung, |
|
Ergebnis: |
Petroleumlämpchen |
5b.Temperaturverteilung in einer Flamme
a. Qualitative Untersuchung der Temperaturverteilung
1.
Ein Holzstäbchen wird mit den Zeigefingern der beiden Hände schnell von
oben in den unteren Teil der rauschenden Brennerflamme gebracht und nach
kurzer Zeit wieder hochgezogen.
Es sind zwei leicht verkohlte Streifen (vom Flammenrand) auf dem Holz zu
sehen.
2.
Ein Holzstäbchen wird wie bei 1. nur in den oberen Teil der Flamme
gehalten.
Jetzt ist nur noch eine, dafür aber stark verkohlte Stelle auf dem Holz
zu sehen.
(Die Versuche 1 und 2 können auch mit einem Magnesiastäbchen zwischen den Zeigefingern durchgeführt werden. Dann hat man mehr Zeit und kann die heißesten Stellen durch helles Glühen des Stäbchens ausfindig machen)
3. Ein Streichholz wird schnell mit dem Kopf in die Mitte des unteren blauen Kegels der rauschenden Flamme gebracht. Der Kopf entzündet sich nicht, wohl aber wird das Holz selber am Außensaum der Flamme angebrannt. Wartet man zu lange, wird der Kopf von der sich dort bildenden Flamme entzündet.
|
b. Quantitative Untersuchung der
Temperaturverteilung Mit einem (digitalen) Thermometer mit dem Drahtfühler (Vorsicht: die Isolierung nicht in der Flamme verschmoren) werden die einzelnen Flammenbereiche untersucht. Man findet im unteren Bereich der Flamme innen Temperaturen um 200-300°C, außen um 400-600°C; im oberen Bereich der Flamme bis über 1000°C. |
|

Das Bild ist entlehnt: http://www.betriebsfeuerwehr.ch/ausbildung/brandverhalten.htm
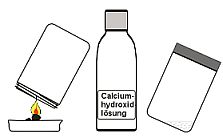
5c Was geschieht chemisch beim Brennen der Kerze?
Man spricht bei Kerzen oft von Paraffin-Wachs. Der Lehrer erklärt uns, das Paraffine sogenannte KW's sind. Sie sind aufgebaut aus Kohlenstoffen und Wasserstoffen. Also testen wir dies. Die Reaktions-produkte: Aus Kohlenstoff entsteht bei der Verbrennung Kohlenstoffdioxid (Kalkwasserprobe) aus Wasserstoff entsteht bei der Verbrennung mit Sauerstoff Diwasserstoffoxid, besser bekannt als Wasser (WATESMO-Probe).
|
Nachweis von Wasser und Kohlenstoffdioxid bei Verbrennungen
|
mit einer Kerze! |
 Film: L01a |
5d. Wird die Kerze (incl. Produkte) beim Verbrennen leichter?
Feuer löschen ist nichts anderes als dafür zu sorgen, dass mindestens eine der drei Bedingungen für Feuer nicht erfüllt ist.
1. genügend
brennbarer Stoff
2. genügend
brandfördernder Stoff
3. Die Entzündungstemperatur muss
erreicht sein
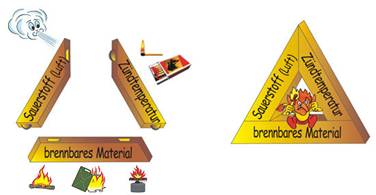
6a Das Feuerdreieck
Das Feuerdreieck ist ein Begriff der Feuerwehr aus dem Brandschutz
Brandklassen und Feuerlöscher
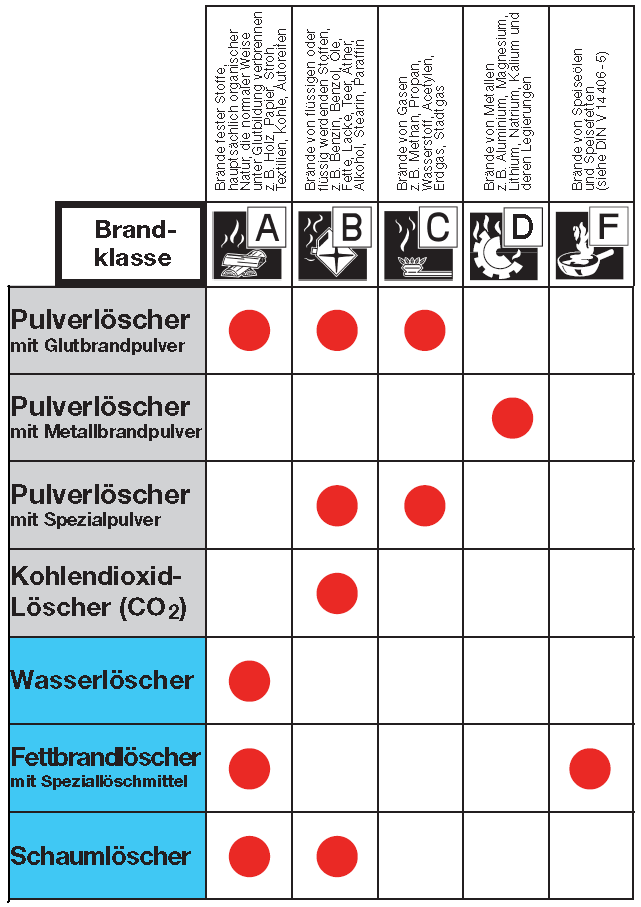
6b Beispiele für Feuerlöschen
a. Wenn man beim Brenner das Gas abdreht, ist Bedingung 1 (brennbarer Stoff) nicht mehr erfüllt
b. Wenn man ein Holzfeuer mit Wasser löscht, ist Bedingung 3 (Entzündungstemperatur muss erreicht sein) nicht mehr erfüllt.
c. Bei Waldbränden schlägt man vorher Schneisen (Zonen, in denen dann keine Bäume mehr stehen). Damit ist für das ankommende Feuer Bedingung 1 (brennbarer Stoff) nicht mehr erfüllt.
d.
Ausblasen einer Kerze: Die brennenden
Dämpfe werden unter den Entzündungspunkt abgekühlt.
(Bedingung 3) Zusätzlich werden sie aber auch noch verweht. (Bedingung
1)
e. Ausdrücken einer Kerze: Abgesehen davon, dass man sich dabei die Finger verbrennen kann, ist der Grund fast derselbe wie beim Ausblasen. Der Docht wird dadurch extrem abgekühlt.
f.
Wieso lassen sich Scherzkerzen nicht
ausblasen?
In den Docht ist Magnesium verarbeitet, das nach dem Ausblasen der
Flamme noch sehr heiß weiter glüht. Diese Temperatur (von mehr als 250
Grad) reicht aus, um die noch warmen Paraffin-Dämpfe wieder zu entzünden
6c.
Feuerlöschen
|
Prinzip |
|
|
Materialien |
3 Bechergläser, 800 mL hohe Form |
|
Chemikalien |
2 Teelichte, Kohlenstoffdioxid (Stahlflasche) |
|
Skizze |
entfällt |
|
Durchführung |
Wir geben in zwei Bechergläser je ein angezündetes Teelicht und
füllen das dritte Becherglas mit Kohlenstoffdioxid aus der
Stahlflasche. |
|
Ergebnis: |
Kohlenstoffdioxid löscht die Teelichtflamme. |
6d Löschen von Benzinbränden
Film: A14f |
|
|
Durchführung Beobachtung: |
Leichtbenzin Herr Diplom-Chemiker Dr. Franz Kappenberg versucht den Benzinbrand in einer Porzellanschale mit Wasser aus einer Spritzflasche zu löschen. Alles sieht ganz harmlos aus. Es funktioniert nicht. |
|
Erklärung: |
Es klappt nicht, weil das Benzin auf dem Wasser schwimmt und einfach weiter brennt. |
|
Durchführung Beobachtung: |
Schwerbenzin/Öl Schwerbenzin/Öl lässt sich nicht direkt in der Porzellanschale anzünden. Man muss es erst auf einem Dreifuß erhitzen, damit genügend brennbares Gas vorhanden ist. Als der Lehrer diesen Brand mit der Spritzflasche löschen will, gibt es eine 1- 2 Meter hohe Stichflamme und das Öl brennt weiter. Erst ein herbeigerufener Kollege kann mit einem Feuerlöscher (Kohlenstoffdioxid) den Brand löschen. Alle rufen Zugabe, Zugabe... |
|
Erklärung: |
Wenn man Wasser auf das brennende Öl (ca. 300 °C) schüttet, wird das Wasser zu Wasserdampf. Dabei vergrößert sich das Volumen um mehr als das 1000-fache. Das verdampfende Wasser reißt das Öl mit. Es kommt brennendes Öl an ganz vielen Stellen mit brand-fördernder Luft zusammen. Dadurch entsteht eine riesige Stichflamme. Durch das darüber gesprühte Kohlenstoffdioxid ist Bedingung 2 (genügend brandfördernder Stoff - Luft) nicht mehr erfüllt. |
6e Experimente mit der Kupferspirale
|
Durchführung Beobachtung: |
Wir sollen zunächst eine kalte Kupferspirale von oben in die Teelichtflamme halten. Danach sollen wir die Spirale in der Brennerflamme erhitzen und dann wieder in die Teelichtflamme halten. |
|
Erklärung: |
Die Flamme geht aus, weil die Spirale die kalte Metallspirale den Wachsdampf abkühlt (Bedingung 3), evtl. sogar kondensiert (Bedingung 1). Bei der heißen Spirale geschieht beides nicht. |
6f Wer konstruiert den effektivsten Feuerlöscher? Wir!
Unser Lehrer zeigt uns, wie man Kohlenstoffdioxid freisetzen kann.
In einem Becherglas wird zu Sodalösung etwas Salzsäure gegeben: Es sprudelt sehr stark.
Nun sind wir dran: Wir konstruieren den Feuerlöscher:
Material:
Standflasche, Stopfen, Winkelrohr, Spritze mit Nadel und Hahn , Porzellanschale
mit Feuer
Chemikalien: Feuerlöscherlösung, Salzsäure
Zeichnung
Wie der Feuerlöscher funktioniert
Wir geben mit der Spritze Salzsäure zur Lösung und verschließen den Hahn. Es entsteht CO2. Da das Gas nicht entweichen kann drückt es auf die Lösung. Diese spritzt aus der Flasche und löscht das Feuer.
Geben wir Spüli-Schaum in die Lösung passiert das Gleiche; aber wir haben nun einen Schaumlöscher.
7a Quizfrage für Schlaue Köpfe: Welche Kerze erlischt zuerst?
 Film: A14O |
|
|
Durchführung / Beobachtung: |
Zwei Kerzen werden in unterschiedlicher Höhe in einem Gurkenglas aufgebaut und entflammt. Dann wird das Glas mit dem Deckel verschlossen.... |
|
Ergebnis: |
??? |
7b Feuerspucken
 Film: A14P |
|
|
Durchführung / Beobachtung: |
Auch feste Stoffe können eine große Oberfläche haben, wenn sie klein genug sind. |
7c Feuertornado
 Film: A14Q |
|
|
Durchführung / Beobachtung: |
Durch Drehung des Metallgitters wird der
Kamineffekt verstärkt. |
7d. Feuerspirale
 Film: A14R |
|
|
Durchführung / Beobachtung: |
Benzindampf sinkt im Schlauch herunter, bis er von einem Teelicht angezündet wird..... |
7e. Benzinexplosion im Filmdöschen
 Film: A12 |
|
|
Durchführung / Beobachtung: |
Benzin wir in einem kleinen Filmdöschen "vergast" und lässt sich mehrfach zünden. |
7f. Feuerzeuggas-Rakete
 Film: A13 |
|
|
Durchführung / Beobachtung: |
Ein Feuerzeuggas-Luft-Gemisch wird in einer Flasche gezündet. Der entstehende Druck presst das Wasser heraus. Durch diesen Rückstoß fliegt die Rakete besonders hoch in die Luft. |